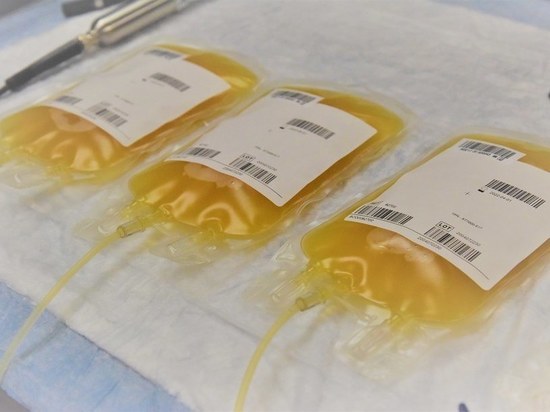
Плазма состоит главным образом из воды, белков и свертывающих веществ. Ее получают из крови путем извлечения из нее белых и красных кровяных телец. Плазма, выделенная из донорской крови, подвергается шоковой заморозке в течение 24 часов после забора. Замороженная плазма хранится при температуре -25°C (и более низкой) на протяжении трех лет. Лечение плазмой широко применяется еще с конца XIX века – для пациентов с инфекционными, аутоиммунными, неврологическими заболеваниями, ее также переливают при нарушениях функции свертываемости крови и для восполнения массивных кровопотерь. Смысл переливания в том, чтобы «запустить» иммунную систему инфицированного пациента, чтобы он мог бороться с COVID-19 до тех пор, пока его организм не сгенерирует свои собственные антитела.
Любопытно, что выдача экстренного разрешения от FDA ожидалась ранее, на основании удовлетворительных результатов исследования по программе клинике Мэйо, в рамках которой были сделаны переливания плазмы более чем 70 тысячам пациентов с COVID-19. Исследование показало, что плазма оказала некоторое влияние на снижение смертности среди госпитализированных пациентов с коронавирусом. Отмечается, что лечение плазмой больше всего помогло наиболее уязвимой группе инфицированных – людям старше 80 лет, которые не были на аппаратах искусственного дыхания (ИВЛ). Кроме того, принимая решение о выдаче экстренного разрешения, руководство FDA опиралось на опыт испытаний в других странах, в том числе и в Китае. Комиссар FDA Стивен Хан сообщил, что пациенты не испытывали негативных последствий, что свидетельствует о безопасности такого лечения.
На совместной пресс-конференции с президентом Трампом Хан отметил, что исследовательская программа Mayo Clinic пользуется поддержкой федерального правительства и с апреля лечит пациентов плазмой выздоравливающих. Было зарегистрировано более 100 тысяч пациентов с COVID-19, и около 70 тысяч пациентов прошли курс лечения. Переломным моментом в принятии решения о выдаче экстренного разрешения, по словам Хана, стало то, что среди пациентов, которых лечили плазмой с наиболее высокими титрами антител, «выживаемость увеличилась на 35%. Это означает, что из 100 больных человек 35 (были бы) спасены с помощью плазмы выздоравливающих».
Однако исследование не было рецензировано и не включало контрольную группу, что затрудняло интерпретацию данных.
Тем не менее в процесс выдачи экстренного разрешения 19 августа вмешались руководители государственных органов здравоохранения, включая главу Национальных институтов здоровья (NIH) доктора Фрэнсиса Коллинза и главного инфекциониста доктора Энтони Фаучи. Они призвали к осторожности, сославшись на недостаточные данные исследования о пользе и вреде лечения коронавируса плазмой. Выдача разрешения была приостановлена. Администрация Белого дома тогда выдвинула предположение, что это решение было «политически мотивированным».
И вот с почти недельной задержкой FDA все-таки выдало разрешение на это лечение. В заявлении FDA сообщается: «Разумно полагать, что плазма, полученная из крови переболевших COVID-19, может быть эффективной для уменьшения тяжести или сокращения продолжительности заболевания у некоторых госпитализированных пациентов, а преимущества перевешивают риски». FDA также добавило, что плазма переболевшего COVID-19 с «высоким титром антител» может быть эффективной для снижения смертности госпитализированных пациентов, но также, по усмотрению госпиталя, может использоваться и плазма с низким титром.
В то же время, комментируя это решение, бывший комиссар FDA Скотт Готлиб заявил, что плазма «вероятно, немного полезна» в лечении коронавируса, но представители здравоохранения «хотели бы получить более точные данные, чтобы выдать окончательное заключение».
Экстренное разрешение на использование действительно не равняется окончательному одобрению того или иного лечебного средства или метода терапии. Врачи, работающие напрямую с коронавирусными пациентами, отмечают, что с получением экстренного разрешения FDA станет меньше волокиты с оформлением бумаг на назначение лечения плазмой. В то же время до сих пор остаются несколько вопросов: на какой фазе лечения лучше проводить инфузию; одинакова ли плазма, полученная от всех переболевших, или важно количество антител; насколько она эффективна. Проблема в том, что доказательства эффективности и надлежащей дозировки плазмы остаются пока неубедительными: испытания проводятся с задержками, есть проблемы с поисками добровольцев для сдачи крови. Поэтому представители FDA отмечают: крайне важно, чтобы люди, выздоровевшие от коронавируса, сдавали кровь для помощи другим. В противном случае высока вероятность того, что у нас будет дефицит плазмы и не все пациенты смогут получить это лечение. Напомним, что, по данным университета Джонса Хопкинса, на данное время коронавирусом переболели уже более 2 миллионов американцев.